Мацей Пржудзик1· Михал Боровик1 · Мирослав Лешув1 · Роман Лешув1
Аннотация
Введение Полипропиленовые материалы в настоящее время широко используются для лечения различных урогинекологических заболеваний. Тем не менее, изредка этот вид лечения может сопровождаться осложнеииями – эрозированием имплантатов в мочевой пузырь или мочеиспускательный канал. Стандартного лечения таких осложнений не существует. Мы представляем наш опыт в области чреспузырных лапароэндоскопических операций (T-LESS) по удалению эрозирующих материалов и обзор литературы в этой области.
Методы и материалы. С июня 2015 года по май 2017 года восемь женщин (средний возраст 66,5 лет, диапазон – 55–80 лет) были направлены в наш Центр из-за эрозирования полипропиленового материала в мочевой пузырь после операции по поводу недержания мочи или лечения опущения тазовых органов. Пациентам поставили диагноз на основе УЗИ и цистоскопии. Обнаружено семь эрозирований в мочевой пузырь и одна пенетрация в мочевой пузырь и уретру. Пациентам назначено удаление материала с использованием метода T-LESS. Использовался одноразовый набор Tri-Port+ и стандартные лапароскопические инструменты. Эрозированные материалы рассекали и вырезали, а дефекты стенки мочевого пузыря закрывали шовным материалом с "насечками". Проведена оценка периоперационной эффективности и безопасности метода, запланированы последующие посещения пациентов через 6 недель и через каждые 3 месяца после процедуры. Пациентам предложен цистоскопический осмотр в течение 7–10 месяцев после операции.
Результаты Процедуры успешно выполнены у всех пациенток. Никакой кровопотери или осложнений не наблюдалось. Среднее время операции составило 54,5 минуты, а среднее время пребывания в стационаре – 30 часов. В течение 11 месяцев наблюдения все пациентки были излечены, кроме одной, у которой была эрозия мочеиспускательного канала.
Выводы T-LESS техника удаления эрозированных сеток является безопасной и эффективной. Точный доступ к мочевому пузырю сводит к минимуму травматичность, а сшивание дефектов стенки мочевого пузыря может снизить риск рецидива.
Ключевые слова Недержание мочи, Хирургия, Осложнения, Лапароэндоскопическая однодоступная хирургия
Введение
Использование полипропиленовых материалов – стандартный метод лечения стрессового недержания мочи и опущения тазовых органов с 1995 года, когда Ульмстен и Петрос представили тканевую ленту свободной синтетической петли (TVT) для установки средне-уретрального слинга. Это произвело революцию в терапии недержания мочи [1]. Высокий показатель успеха средне-уретральных слингов дает возможность хирургам восстанавливать опущение тазовых органов с помощью полипропиленовой сетки [2].
Несмотря на то, что отдаленные результаты удовлетворительные, такие процедуры связаны с различными осложнениями, в том числе такими серьезными, как перфорация кишечника [3]. Другие типы осложнений включают перфорацию мочевого пузыря, повреждение сосудов, инфекцию мочевыводящих путей, задержку мочи, чрезмерную первичную гиперактивность детрузора, хроническую боль в области таза и эрозирование сетки во влагалище, мочеиспускательный канал или мочевой пузырь [4–8].
Присутствие эрозированнного материала в мочевом пузыре требует тщательного выбора оптимального варианта лечения. Общий зарегистрированный уровень эрозирования ленты и сетки в мочевом пузыре низкий (около 0,5–0,6%) [9]. Самой серьезной проблемой среди осложнений является эрозия мочевого пузыря в результате несоблюдения золотого стандарта восстановительной хирургии и, следовательно, рецидив заболевания. Восстановительные операции можно выполнять открытой или эндоскопической трансуретральной или лапароскопической техникой. В настоящее время чаще всего используют открытые подходы.

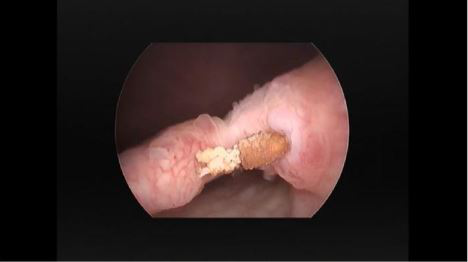
Рис. 1 Образец эрозированной ленты, удаленной у пациента
Недостатки стандартных методов, открытых, лапароскопических или роботизированных подходов, включают относительно высокую травматичность, длительное пребывание в стационаре и неудовлетворительную экономическую эффективность [9, 10]. Следовательно, логичным следствием этого стало использование других минимально инвазивных технологий, либо трансперитонеальных, либо трансвезикальных однопортовых методов, которые были введены в урологическую практику Ране и др. и Ингбером и др. в 2008–2009 гг. [11, 12]. Здесь мы представим свои клинические результаты у восьми пкциентов, перенесших операцию с использованием трансвезикальной, лапароэндоскопической, однопортовой хирургии (T-LESS) для удаления хирургических материалов, которые подверглись эрозированию в мочевом пузыре. Литературы по применению однопортовой хирургии для лечения эрозирования мало. Поэтому мы рассмотрели и сравнили результаты нашей группы с материалами, представленными другими исследователями.
Методы и материалы
С июня 2015 года по май 2017 года восемь женщин в возрасте 66,5 лет (от 55 до 80) со средним ИМТ 28,4 (21,09–42,75) были направлены в наш Центр из-за эрозирования полипропиленового материала в мочевой пузырь после операции по поводу недержания мочи или лечения опущения тазовых органов (рис. 1). У одной женщины наблюдалось постоянное стрессовое недержание мочи (СНМ), а у двух пациентов были диагностированы симптомы первично возникшей ургентности.
Две пациентки прошли безрезультатное трансуретральное лечение. Подробные данные о пациентах представлены в Таблице 1. Независимо от материала, его размера и положения в мочевом пузыре, всем пациентам предписано проведение операции с использованием однопортовой методики. Мы выбрали эту методику на основе опыта Центра и значительного сокращения времени операции по сравнению со стандартной лапароскопической техникой.
Операция начиналась со стандартной цистоскопии, при которой мы наполняли мочевой пузырь физиологическим раствором – 300–400 мл (в зависимости от объема мочевого пузыря). Разрез кожи 15–25 мм производился на 2 см выше лобкового симфиза. В большинстве случаев требовалась дополнительная инцизия фасции прямой мышцы
живота. Фабричный порт (Tri-Port +, Olympus, Германия) (рис. 2а, б) вводился через разрез кожи непосредственно в мочевой пузырь под контролем цистоскопа, без дополнительного разреза стенки мочевого пузыря. Такой контроль делает установку порта более безопасной, поскольку кончик порта визуально отслеживается в момент проникновения в мочевой пузырь (рис. 2а, б). Никаких особых мер предосторожности не требовалось. Когда троакар входил в мочевой пузырь, внутреннее кольцо Tri-Port+ сдвигалось вниз. Троакар извлекали, и оба кольца системы соединялись вместе и фиксировались к брюшной стенке. Жидкость из мочевого пузыря эвакуировалась, создавался пневмовезикум с углекислым газом до 14 мм рт. Ни в одной из процедур не наблюдался везикоуретральный рефлюкс газа.
Внутрипузырную часть сетки с фрагментами, которые подлежали удалению из дна мочевого пузыря, иссекали и удаляли.
У шести пациенток дефекты стенки мочевого пузыря были закрыты с помощью нити V-Loc (Covidien, США) (рис. 3a–c). Апоневроз и кожа были ушиты двумя швами. Катетер Фолея вводили трансуретрально и оставляли на 5–9 дней. Антибиотикопрофилактика (фторхинолоны и цефалоспорины) проводилась до и после операции. Период лечения зависел от активного или постоянного инфицирования мочевыводящих путей, на основе результатов микробиологического исследования.
Таблица 1 Демографические данные и результаты
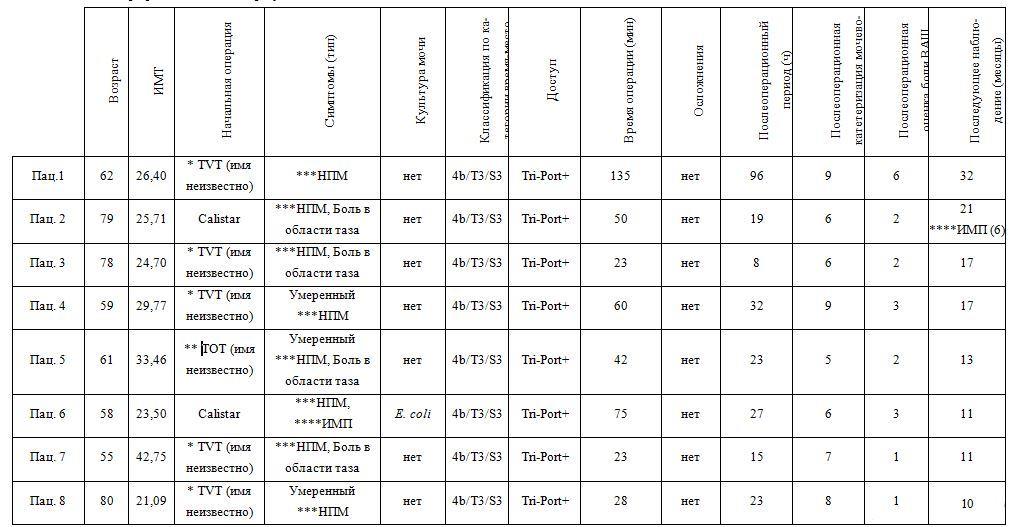
* TVT – свободная синтетическая петля
** ТOT– трансобтураторное проведение слинга
*** НПМ – неотложный позыв к мочеиспусканию
****ИМП – инфекция мочевыводящих путей
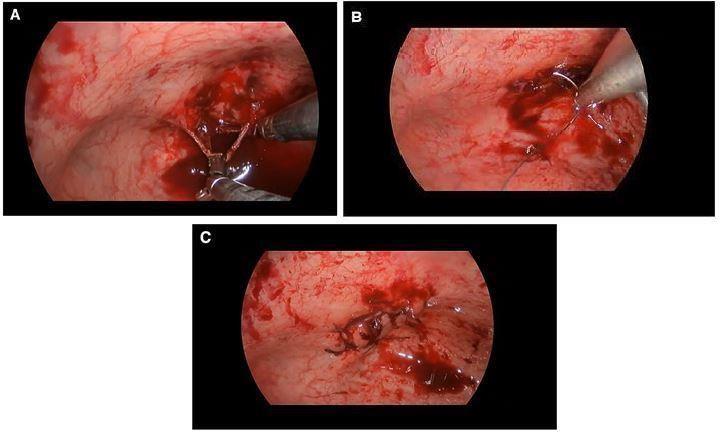

Рис.2. Чрескожное надлобковое введение устройства Tri-Port +. Введение Tri-Port + через разрез кожи 1,5 см. b Тупое введение порта через стенку мочевого пузыря
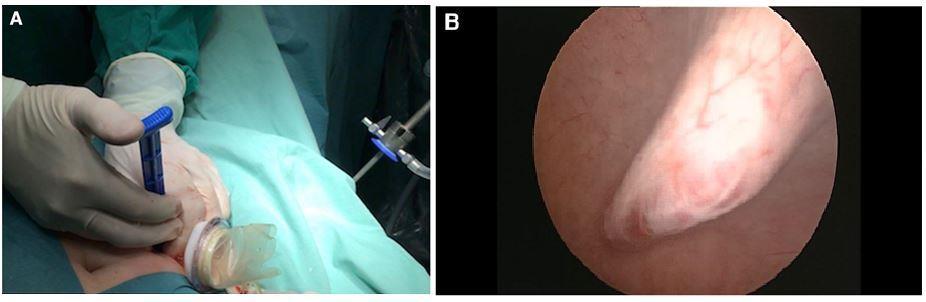
Рис. 3 Этапы операции. Вытягивание ленты и рассечение стандартными лапароскопическими инструментами. b Закрытие дефекта стенки мочевого пузыря с помощью стежка. c Вид после наложения швов
Во всех операциях трансуретральный доступ использовался для захвата или аспирации. Для оценки послеоперационной боли использовалась визуальная аналоговая шкала. В рамках контрольного обследования выполнялось УЗИ брюшной полости, общее обследование и посев мочи через 6 недель и 6 месяцев после операции. Для исключения таких осложнений, как кровоизлияние в тазовую область, гидронефроз и образование камней использовалась ультрасонография. Кроме того, пациенты обследованы с помощью цистоскопии, за исключением тех, кто отказался от обследования.
Поиск проводился по базе PubMed с использованием ключевых слов «средне-уретральный слинг», «трансвагинальная сетка», «эрозия сетки», «эрозия мочевого пузыря», «однопортовая лапароскопия» и «лапароэндоскопическая однопортовая хирургия» по всей доступной литературе на английском языке с января 2005 г. по март 2018 г. Статьи выбраны в соответствии с темой, т. е. те, которые касаются лечения эрозирования мочевого пузыря или уретры. Всего найдено 27 статей, в 6 из которых представлен чрескожный чреспузырный доступ.
Результаты
Все процедуры прошли успешно, дополнительный порт не использовался. Переход к открытому методу не был необходим ни в одном из случаев. Среднее время операции составило 54,5 мин (диапазон 23–135 мин), а средняя послеоперационная госпитализация составила 30 ч (диапазон 8–96 ч). Кровопотеря была минимальной во всех процедурах. Пациентки получали пероральные приемы пищи в первый послеоперационный день.
В течение 6 месяцев наблюдения (от 3 до 10 месяцев) не было отмечено рецидива эрозии мочевого пузыря, хотя у пациентки 3 наблюдалось выдавливание остаточной ленты в уретру. Это было следствием неполного удаления эрозированной кальцифицированной ленты во время трансуретральной операции, выполненной до направления в наш центр. У этой пациентки T-LESS доступ к мочеиспускательному каналу был неэффективным, потому что после удаления ленты мы не смогли зашить отверстие стенки мочеиспускательного канала, и лишь коагулировали кровоточащие сосуды. Мы хотели бы подчеркнуть, что это состояние было бессимптомным и было обнаружено при контрольной цистоскопии.
Ни одна из пациенток не показала положительный посев мочи в отдаленном периоде. Более того, такие симптомы, как рецидивирующее недержание мочи или неудержание не наблюдались.
Результаты обзора литературы представлены в таблице 2 и подробно описаны в разделе «Обсуждение».
Обсуждение
Недержание мочи является очень распространенной проблемой и затрагивает до 50% женщин в определенный момент их жизни [16]. Из пациенток, перенесших установку полипропиленовой ленты для лечения стрессового недержания мочи (SUI), 9,8% испытывают осложнения, связанные с процедурой [16]. Такие осложнения как эрозия мочевого пузыря или уретры самые сложные в лечении. Эрозирование сетки в мочевой пузырь проявляется в виде полного или частичного прободения ленты или сетки в стенку мочевого пузыря, обычно они проникают в полость мочевого пузыря и кальцифицируются [17].
Хотя большинство авторов согласны с тем, что эрозированные материалы необходимо удалять, нет единого мнения относительно того, какой метод для этого предпочтительнее [9, 18, 19]. Авторы представили отдельные случаи эрозии мочевого пузыря у небольшого числа пациентов [4–8, 20]. Эрозированный материал обычно удаляют с использованием открытой техники. Такой подход значительно уменьшает симптомы, но является инвазивным и может вызвать рецидив недержания мочи [2, 20].
Метод трансвезикального лапароскопического удаления сетки из мочевого пузыря был представлен Сарлосом [22], который вылечил с его помощью 7 пациентов и показал, что метод эффективен и безопасен. Рупре и др. сообщили о лапароскопическом удалении эрозированных материалов у 9 женщин и показали, что метод является безопасным и выполнимым, но в некоторых случаях приводит к повышенному риску повторного недержания мочи. Они также пришли к выводу, что удаление всего имплантированного материала не является необходимым и может не повлиять на состояние удержания мочи у пациента [18].
Таблица 2 Обзор литературы по удалению надлобковой однопортовой сетки с января 2005 года по март 2018 года (N = 6)
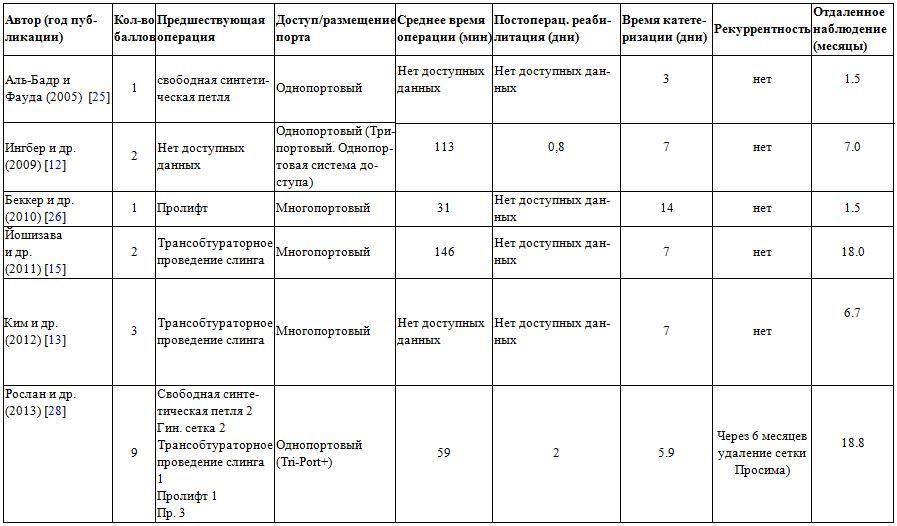
Для устранения эрозии мочевого пузыря применялись различные трансуретральные эндоскопические методы с применением либо лазерной коагуляции, либо электрокоагуляции. Эти подходы являются минимально инвазивными, с коротким пребыванием в стационаре, но они связаны со значительной частотой рецидивов [23, 24].
Как открытый, так и лапароскопический подходы кажутся слишком инвазивными для удаления относительно небольших фрагментов имплантированных материалов. Продолжительность госпитализации превышает 6 дней, а в некоторых случаях возникают осложнения [18]. Аль-Бадр и Фуда успешно вырезали часть ленты свободной синтетической петли, проникшей в мочевой пузырь с помощью ножниц, которые они вводили через лапароскопический порт прямо в мочевой пузырь [25]. Беккер и др. следовали методике Аль-Бадра, и вырезали эрозированную сетку без ушивания дефектов мышечного слоя мочевого пузыря [26]. Чтобы закрыть дефекты стенки мочевого пузыря швами, Йошизава и др., а также Ким и др. использовали трансвезикальный доступ для многопортовой (3) лапароскопии с удалением проникших материалов [13, 15].
Ингбер и др. в 2009 а также Рослан и др. в 2011 году были первыми, кто выполнил чреспузырную лапароэндоскопическую однопортовую операцию для удаления продуктов эрозии мочевого пузыря [12, 27]. Серия из девяти пациентов, на которых применялся этот подход, была представлена в 2012 году Росланом и др. [28]. Авторы достигли хороших результатов, с рецидивом только у одного пациента. Среднее время операции составило 59 минут, а пребывание в стационаре – 2,4 дня [28].
Эти результаты побудили нас представить данную инновационную методику, которая казалась привлекательной из-за ее минимальной инвазивности. Поскольку мы являемся специализированным медицинским центром, у нас был опыт нескольких случаев с эрозированием мочевого пузыря, которые мы оперировали с помощью открытой техники. Мы заметили, что риск такого типа доступа слишком велик по сравнению с реальной серьезностью заболевания. Таким образом, мы решили изменить подход к удалению сеток, проникающих внутрь мочевого пузыря и, наконец, убедиться, что новая чреспузырная однодоступная операция может быть хорошим и надежным вариантом для решения проблем с эрозиями мочевого пузыря.
Поэтому мы применили менее инвазивный метод, который позволяет либо удалять эрозированные материалы, либо зашивать дефекты стенки пузыря.
В нашем пуле пациенток результаты были аналогичны результатам, представленным другими авторами (таблицы 1, 2), хотя в нашей группе время госпитализации было в 2 раза меньше, чем в предыдущих сообщениях. Пребывание в стационаре 30 ч и время операции 54,5 мин подтверждают минимальную инвазивность и безопасность метода.
В нашей группе цистоскопия проведена 6 женщинам. Пациенты 2 и 6 отказались от обследования из-за отсутствия симптомов.
Процедура T-LESS характеризуется превосходной визуализацией операционного поля в мочевом пузыре и осуществимостью внутрипузырного ушивания, которое невозможно выполнить через трансуретральный доступ. Дополнительные преимущества – минимальная послеоперационная боль и возможность использования стандартных лапароскопических инструментов, которые можно вводить трансуретрально упрощают процедуру и сокращают время операции. Мы предполагаем, что закрытие дефекта стенки мочевого пузыря может снизить риск образования свища.
Еще одна проблема заключается в продолжительности катетеризации мочевого пузыря. В нашей группе длительность дренирования мочевого пузыря катетером зависела от типа удаляемого материала, ширины дефекта стенки мочевого пузыря.
Наконец, мы предполагаем, что установка мочевого катетера на 5 дней достаточна для пациентов с небольшими или сшитыми отверстиями в стенке мочевого пузыря. Кроме того, при определении времени катетеризации учитывалось расстояние до места проживания пациента.
Ограничениями этой работы являются небольшое количество пациентов и короткое время наблюдения. У нас не было группы для сравнения, потому что описанное состояние довольно необычно, и мы сосредоточились на применимости и безопасности техники T-LESS.
Мы понимаем, что этот метод достаточно инновационный, и его полезность еще не оценена полностью. Тем не менее, такой подход представляет потенциал для снижения инвазивности и частоты рецидивов лечения ухудшающегося состояния.
Только результаты многоцентровой группы могут дать более надежный результат; Однако наш опыт показывает, что процедура T-LESS может быть хорошим решением проблем открытых или лапароскопических процедур.
Выводы
Чреспузырное лапароэндоскопическое однопортовое удаление хирургических материалов, извлекаемых из мочевого пузыря является безопасной, эффективной, воспроизводимой и малоинвазивной процедурой. Эта процедура предполагает относительно короткое время операции, быстрое выздоровление и хороший косметический эффект и позволяет использовать как стандартные, так и сложные лапароскопические инструменты. Этот метод должен рассматриваться, в частности тогда, когда место локализации инородного тела не подходит для эндоскопических процедур или требуется внутрипузырное ушивание. Однако, чтобы способствовать более широкому распространению этого метода необходимы дальнейшие исследования, новый опыт и разработка новых технологий.
Список литературы
1. Ulmsten U, Petros P (1995) Intravaginal slingplasty (IVS): an ambulatory surgical procedure for the treatment of female urinary incontinence. Scand J Urol Nephrol 29:75–82
2. Cosson M, Caquant F, Collinet P et al. Prolift mesh (Gynecare) for pelvic organ prolapse surgical treatment using the TVM group: a retrospective study of 687 patients. Communication in the ICS Meeting Montreal, 31 Aug 2005
3. Peyrat L, Boutin JM, Bruyere F et al (2001) Intestinal perfora-tion as a complication of tension-free vaginal tape procedure for urinary incontinence. Eur Urol 39:603–605
4. Sergouniotis F, Jarlshammar B, Larsson PG (2015) Urethral com-plications after tension-free vaginal tape procedures: a surgical management case series. World J Nephrol 4(3):396–405
5. Parekh MH, Minassian VA, Poplawsky D (2006) Bilateral bladder erosion of a transobturator tape mesh. Obstet Gynecol 108(3 Pt 2):713–715
6. Forzini T, Viart L, Alezra E, Saint F (2015) Erosive complications of mid urethral slings (MUS): 10 years of surgical experience. Prog Urol 25:240–248
7. Wohlrab K, Erekson AE, Myers D (2009) Postoperative erosions of the Mersilene® suburethral sling mesh for antiincontinence surgery. Int Urogynecol J Pelvic Floor Dysfunct 20(4):417–420 \ 8.\ Kasyan G, Abramyan K, Popov AA et al (2014) Mesh–related and intraoperative complications of pelvic organ prolapse repair. Cent Eur J Urol 67(3):296–301
9. Costantini E, Lazzeri M, Porena M (2007) Managing complica-tions after midurethral sling for stress urinary incontinence. EAU-EBU Update Ser 5:232–240
10. Ahmed K, Ibrahim A, Wang TT et al (2012) Assessing the cost effectiveness of robotics in urological surgery—a systematic review. BJU Int 110:1544–1556
11. Rane A, Rao P, Rao P (2008) Single-port access nephrectomy and other laparoscopic urologic procedure using a novel laparoscopic port (R-port). Urology 72(2):260–263
12. Ingber M, Stein R, Rackley R et al (2009) Single-port transvesical excision of foreign body in the bladder. Urology 74:1347
13. Kim JH, Doo SW, Yang WJ, Song YS (2012) Laparoscopic trans-vesical excision and reconstruction in the management of mid-urethral tape mesh erosion and stones around the bladder neck: initial experiences. BJU Int 110:1009–1013
14. Macedo FI, O’Connor J, Mittal VK, Hurley P (2013) Robotic removal of eroded vaginal mesh into the bladder. Int J Urol 20:1144–1146
15. Yoshizawa T, Yamaguchi K, Obinata D, Sato K, Mochida J, Taka-hashi S (2011) Laparoscopic transvesical removal of erosive mesh after transobturator tape procedure. Int J Urol 18:861–833
16. Ford AA, Rogerson L, Cody JD, Ogah J (2015) Mid-urethral sling operations for stress urinary incontinence in women. Cochrane Database Syst Rev 1(7):CD006375
17. Haylen BT, Freeman RM, Swift SE et al (2011) An International Urogynecological Association (IUGA)/International Continence Society (ICS) joint terminology and classification of the com-plications related directly to the insertion of prostheses (meshes, implants, tapes) and grafts in female pelvic floor surgery. Int Uro-gynecol J 22:3
18. Rouprêt M, Misraï V, Vaessen C et al (2010) Laparoscopic surgi-cal complete sling resection for tension-free vaginal tape-related complications refractory to first-line conservative management: a single centre experience. Eur Urol 58:270
19. Chan G, Mamut A, Martin P, Welk B (2016) Holmium:YAG laser ablation for the management of lower urinary tract foreign bod-ies following incontinence surgery: a case series and systematic review. J Endourol 30(11):1252–1261
20. Volkmer BG, Nesslauer T, Rinnab L et al (2003) Surgical inter-vention for complications of tension-free vaginal tape procedure. J Urol 169:570–574
21. Clemens JQ, DeLancey JO, Faerber GJ et al (2000) Urinary tract erosions after synthetic pubo-vaginal slings: diagnosis and man-agement strategy. Urology 56(4):589–594
22. Sarlos D, Aigmueller T, Schaer G (2015) A technique of laparo-scopic mesh excision from the bladder after sacrocolpopexy. Am J Obstet Gynecol 212(3):403.e1–403.e3
23. Ogle CA, Linder BJ, Elliott DS (2015) Holmium laser excision for urinary mesh erosion: a minimally invasive treatment with favorable long-term results. Int Urogynecol J 26(11):1645–1648 24\.\ Barski D, Deng DY. Management of mesh complications after SUI and POP repair: review and analysis of the current literature.
BioMed Res Int 2015;2015;831285
25. Al-Badr A, Fouda K (2005) Suprapubic-assisted cystoscopic exci-sion of intravesical tension-free vaginal tape. J Minim Invasive Gynecol 12(4):370–371
26. Bekker MD, Bevers RF, Elzevier HW (2010) Transurethral and suprapubic mesh resection after Prolift® bladder perforation: a case report. Int Urogynecol J 21(10):1301–1303
27. Roslan M, Markuszewski M, Gibas A et al (2011) Laparoendo-scopic single-site transvesical removal of mid-urethral polypro-pylene sling eroded into the bladder. Videosurgery Other Miniin-vasive Tech 6(2):111–114
28. Roslan M, Markuszewski MM (2013) Transvesical laparoendo-scopic single site surgery to remove surgical materials penetrating the bladder: Initial clinical experience in 9 female patients. J Urol 190(3):909–915
